警惕!这三类心力衰竭药物易导致高钾血症
肾素-血管紧张素系统抑制剂(RASi)、血管紧张素受体脑啡肽酶抑制剂(ARNI)、盐皮质激素受体拮抗剂(MRA)等是心力衰竭治疗的基石药物,但可诱发高钾血症。发生高钾血症的心力衰竭患者死亡风险和再住院风险显著增加,而减少或停用这些药物对心力衰竭患者预后的危害又超过高钾血症带来的风险。为了更好地降低心力衰竭人群中高钾血症的发生风险并规范管理,由中国医师协会心血管内科医师分会、中国老年医学学会心电与心功能分会组织相关专家制定了《心力衰竭药物相关高钾血症防治专家共识》,主要包括心力衰竭患者中高钾血症的流行病学,心力衰竭治疗药物的规范应用,心力衰竭患者合并高钾血症高危人群的识别、监测、随访及预防,降钾用药策略等,以期为临床医师早期预防和管理心力衰竭药物治疗相关高钾血症提供临床依据。
共识六大要点一览
1.高钾血症按严重程度分级,以更好地指导何时及如何调整心力衰竭药物治疗。
2.高钾血症高危心力衰竭患者主要包括:年龄≥65岁、估算肾小球滤过率(eGFR)<45 ml/(min·1.73 m² )、慢性肾脏病 3~5 期 [eGFR<60 ml/(min·1.73 m²)] 合并糖尿病或 NYHA心功能分级Ⅲ ~ Ⅳ级或正在使用肾素-血管紧张素-醛固酮系统抑制剂(RAASi)、既往发生≥2次中度高钾血症或≥1次重度高钾血症的患者。
3.高危人群应低钾饮食,加强血钾监测。
4.RASi/ARNI和MRA是心力衰竭患者发生高钾血症的主要独立危险因素。
5.尽量避免因高钾血症而减量或停用RASi/ARNI和MRA。
6.新型钾离子结合剂有助于RASi/ARNI和 MRA 的规范应用。为避免引起严重的消化道副作用,不建议中期或长期使用聚苯乙烯磺酸钠(SPS)/聚苯乙烯磺酸钙(CPS)。
心力衰竭药物治疗相关高钾血症的发病率高吗?
近年来,多部涉及血钾水平的指南或共识将血钾>5.0 mmol/L 定义为高钾血症,并按血钾水平将高钾血症分为轻度(5.1~5.4 mmol/L)、中度(5.5~5.9mmol/L)、重度(≥ 6.0 mmol/L)高钾血症。
心力衰竭患者中高钾血症的患病率因不同研究入选人群的年龄、基线 eGFR水平以及使用的药物不同而有差别,通常在 4%~18% 之间。
心力衰竭患者合并高钾血症有哪些危害?
1.心力衰竭合并高钾血症的直接危害
(1)对心脏的影响
出现缓慢性心律失常如房室阻滞、窦性心动过缓、窦室传导等,也可出现快速性心律失常如窦性心动过速、室性早搏、室性心动过速和心室颤动。急性严重高钾血症可导致恶性心律失常而威胁患者生命。血钾>6.5 mmol/L时,心律失常风险显著增加,少数患者无心电图的前驱表现而直接猝死。
(2)对肾脏的影响
加快肾脏病进展,持续、反复发生的高钾血症较单次高钾血症可促使血清肌酐升高或增加终末期肾病进展风险。
(3)对骨骼肌的影响
血钾水平为 5.5~7.0 mmol/L 时,可出现肌肉轻度震颤、手足感觉异常;血钾为 7.0~9.0 mmol/L时,可出现肌肉软弱无力、腱反射减弱或消失,甚至出现迟缓性麻痹等。
2.心力衰竭合并高钾血症的间接危害
主要为减量或停用RAASi。高钾血症可导致约70%的心力衰竭患者减量或停用RAASi。研究显示,与血钾正常和较低者相比,伴高钾血症的心力衰竭患者的ACEI或ARB使用率更低。真实世界研究发现,使用低剂量RAASi(<指南推荐剂量的 50%)的心力衰竭患者的主要不良心血管事件和死亡风险分别是使用高剂量RAASi(≥指南推荐剂量的50%)心力衰竭患者的1.86倍和7.33倍。一项美国研究报道也显示,分别有27.7%和30.1%的心力衰竭患者因减量和停用RASi而死亡。
除此之外,高钾血症的发生与心力衰竭患者的不良预后有关。
哪些心力衰竭患者容易发生高钾血症?
高钾血症高危心力衰竭患者主要包括:
(1)年龄≥65岁患者;
(2)eGFR<45 ml/(min·1.73 m² )的患者;
(3)慢性肾脏病 3~5 期 [eGFR<60 ml/ (min·1.73 m²)] 合并糖尿病或 NYHA 心功能分级Ⅲ ~ Ⅳ级或正在使用 RAASi 的患者;
(4)既往发生≥2次中度高钾血症或≥1次重度高钾血症的患者。
哪些心力衰竭治疗药物可导致高钾血症的发生?
部分心力衰竭治疗药物可导致高钾血症的发生风险增加,其中RASi/ARNI和MRA是心力衰竭患者发生高钾血症的主要独立危险因素,机制如表1所示。
表1 可导致高钾血症的常见心力衰竭治疗药物及其主要机制

该如何进行合并高钾血症的心力衰竭患者的用药管理?
应根据血钾水平在合理范围内对心力衰竭治疗药物进行调整,尽量避免因高钾血症而减量或停用RAASi。降钾治疗对于规范心力衰竭用药管理十分关键,对合并高钾血症的患者规范使用心力衰竭治疗药物的同时,应及时启动和维持降钾治疗。
1.RASi/ARNI的规范使用(表 2)
表2 RASi/ARNI 的用药管理策略

(1)建议RASi/ARNI从小剂量启用,逐渐上调剂量,启动和滴定期间监测血钾和肾功能的频率为1次/1~2周,达到最大滴定剂量1~2周后复查,之后1次/月,至稳定后1次/3~6个月。
(2)建议血钾>5.0 mmol/L时启动降钾治疗并维持RASi/ARNI使用,在血钾>6.5 mmol/L或出现高钾血症相关危急情况时,可暂时停用RASi/ARNI。
(3)建议将永久停用RASi/ARNI作为心力衰竭合并高钾血症治疗的最后策略。
2.MRA的规范使用(表3和表4)
(1)启动MRA治疗前应进行血钾监测,血钾≤5.0 mmol/L可启动MRA治疗。如血钾>5.0 mmol/L,应启动降钾治疗,待血钾≤5.0 mmol/L时再启动MRA治疗。
轻度高钾血症患者接受降钾治疗后如需上调MRA剂量,需在1个月后复查血钾水平。中度高钾血症患者接受降钾治疗后,MRA可维持当前剂量但需在1~3个月内复查血钾水平。
对于重度高钾血症患者,应寻找并处理相关诱因,停用MRA 3~5d,给予联合降钾治疗,待血钾恢复至≤5.0 mmol/L后以低剂量重启MRA治疗,并在1个月后复查血钾水平。
表3 基于血钾水平的MRA用药管理策略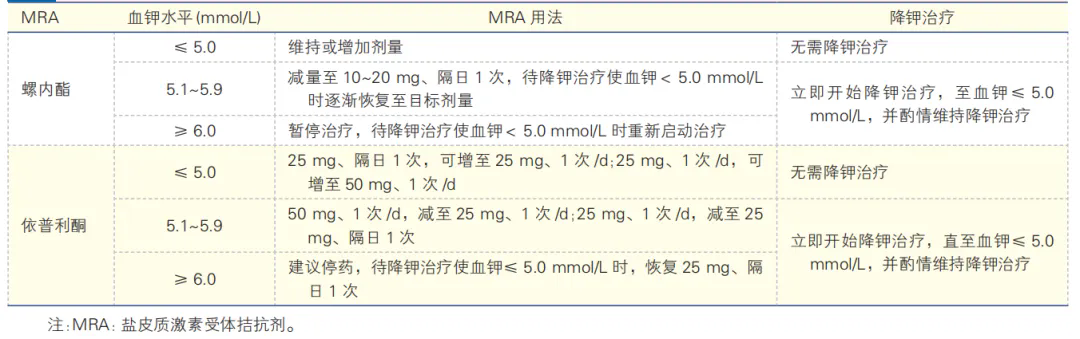
(2)在低剂量MRA治疗下,如血钾水平再次升高,且无其他原因导致血钾≥6.0 mmol/L或eGFR<20 ml/min/1.73m2,建议停止使用MRA。
表4 基于 eGFR 的 MRA 用药管理策略 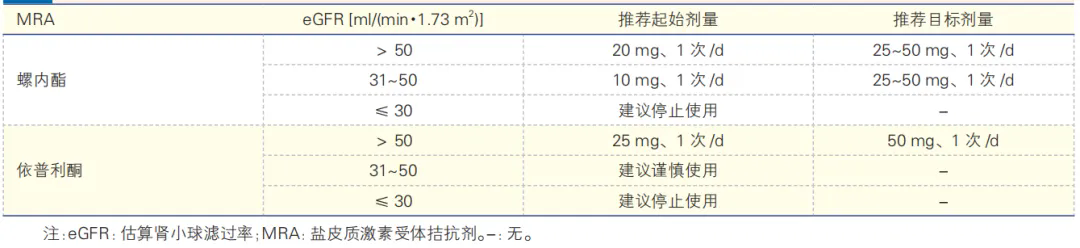
(3)血肌酐>221 μmol/L或eGFR<30 ml/min/1.73m2时,禁用MRA。
3.其他药物的规范使用(表5)
表5 β受体阻滞剂、保钾利尿剂、地高辛治疗的起始和目标剂量 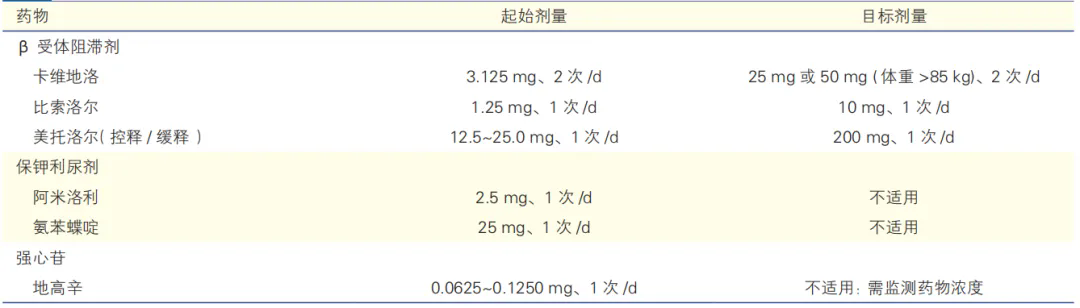
(1)使用β受体阻滞剂、保钾利尿剂前和用地高辛的过程中应定期监测血钾水平。
(2)发生高钾血症时,停止使用地高辛,必要时使用地高辛特异性抗体(Fab)进行治疗。如高钾血症危及生命,应以静脉降钾治疗为基础,联用口服降钾药物如环硅酸锆钠(SZC),待高钾血症被纠正后,经评估后再重新启动地高辛治疗。
高钾血症高危心力衰竭患者该如何进行随访监测?
(1)由于高钾血症的临床症状和心电图表现均缺乏特异性,且患者常无症状,因此所有慢性心力衰竭患者均应定期监测血钾水平。
(2)RASi/ARNI及MRA启动和滴定期间应以1次/1~2周的频率监测血钾和肾功能,达到最大滴定剂量1~2周后复查,之后监测频率1次/月,至稳定后1次/3~6月;
使用袢利尿剂以及肾功能不全的患者应更密切地监测血钾和肾功能,建议1次/1~2月;
对于血钾>5.0 mmol/L或正在服用有血钾升高风险药物的患者,启动袢利尿剂治疗后应密切监测血钾水平。
(3)建议轻度高钾血症患者在3 d内或尽快复查血钾水平,中度高钾血症患者在1 d内复查血钾水平;对于重度高钾血症患者,应立即进行评估和治疗,以确保及时采取必要的措施。
心力衰竭患者该如何预防高钾血症?
(1)适当限制高钾食物摄入,不建议严格控钾饮食。
(2)避免使用非甾体类抗炎药(NSAIDs)、琥珀胆碱、环孢素、肝素和可致血钾水平升高的中药制剂。此外,使用钠葡萄糖共转运蛋白2抑制剂(SGLT2i)并不能预防心力衰竭患者发生高钾血症。
(3)高危患者:对正在服用RAASi或需要调整RAASi剂量的患者以及有其他高钾血症诱因(如服用中药)的患者,推荐尽早使用新型口服钾离子结合剂(如SZC)等药物进行早期预防。
心力衰竭患者发生高钾血症后改如何进行降钾治疗?
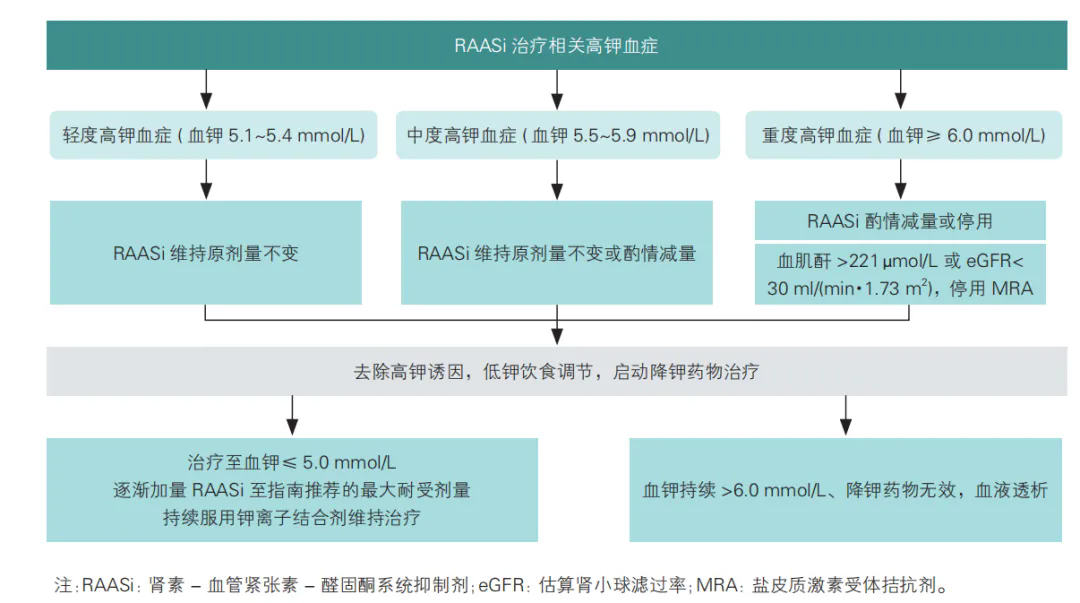
图1 RAASi 治疗相关高钾血症的处理原则
(1)一旦发生高钾血症,应立即停止补钾。
(2)优先选择:缓慢注射10%葡萄糖酸钙10~20 ml或10%氯化钙中心静脉给药1次,直接对抗高血钾对细胞膜极化状况的影响。
(3)次优先级:一次性给予10U短效胰岛素加入50%葡萄糖溶液50 ml静脉输注,随后可给予碳酸氢钠150~250 ml缓慢静脉滴注(碳酸氢钠注射仅推荐用于液体负荷控制达标且合并严重代谢性酸中毒的心力衰竭患者。
➤持续降钾药物治疗
(1)袢利尿剂和噻嗪类利尿剂,如呋塞米静脉注射40~80 mg,肾功能不全时效果欠佳。
(2)阳离子交换树脂如SPS和CPS可促进钾从粪便中排泄。
(3)新型钾离子结合剂SZC可用于高钾血症的纠正阶段和维持治疗阶段,在全胃肠道内高选择性地捕获钾,减少肠道内钾吸收而快速降钾,安全性较高。
表6 常用钾离子结合剂的使用说明 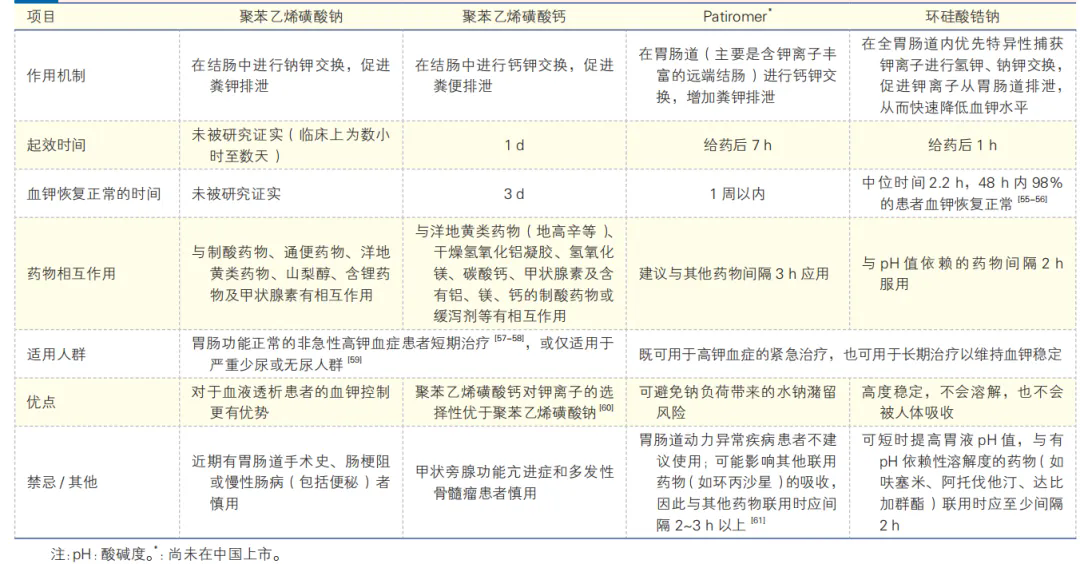
(4)尽量避免停用RAASi,经降钾药物治疗后如血钾持续>5.0 mmol/L,再考虑停用RAASi并继续使用降钾药物。
(5)严重肾功能衰竭或上述治疗方法无效且血钾持续≥6.0 mmol/L时,采用低钾或无钾透析液进行血液透析或腹膜透析。
- 1 【论文写作技巧】90%的论文选题,一开始就选错了:别只盯着"能发",这5个标准才决定你的研究值不值钱
- 2 【论文写作技巧】论文前言总被批逻辑乱?掌握3步7问核心逻辑,新手也能写出高分引言
- 3 十投九中!护理核心期刊推荐与选题攻略,助力高效发文!
- 4 【论文写作技巧】从引言到结论,6种对比论证用法,让你的论文说服力大幅提升
- 5 文献综述写得像流水账?搞懂这3个作用和5个标准,再也不当文献搬运工
- 6 核心期刊发表实用指南:选题定成败,写作重逻辑,投稿要精准
- 7 期刊论文结论写作指南:标准结构+避坑要点一次说清!
- 8 论文数据分析不再难!16类常用法详解,选题写作轻松“抄作业”(下)
- 9 论文数据分析不再难!16类常用法详解,选题写作轻松“抄作业”(上)
- 10 摘要和结论到底啥区别?一篇文章彻底讲清楚,再也不写混!